Botulismo
Il botulismo è una rara ma grave malattia neuro-paralitica acquisita causata dalla tossina botulinica prodotta da clostridi, il più comune è il Clostridium botulinum.[1][2] Casi di botulismo sono stati riportati in Asia, Australia, Europa, Nord e Sud America.[3]
| Botulismo | |
|---|---|
 | |
| Specialità | infettivologia |
| Eziologia | Clostridium botulinum e tossina botulinica |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 005.1, 040.41 e 040.42 |
| ICD-10 | A05.1 |
| MeSH | D001906 |
| MedlinePlus | 000598 |
| eMedicine | 213311 |
Etimologia
[modifica | modifica wikitesto]La malattia prende il nome dal termine latino botulus (salsiccia) perché la sua descrizione fu associata inizialmente al consumo di salsicce preparate in casa.[1]
Storia
[modifica | modifica wikitesto]Clostridium botulinum, il più noto tra i clostridi produttori di tossine botuliniche, è stato descritto per la prima volta nel 1897 da Emile van Ermengem, in seguito a un focolaio di botulismo alimentare verificatosi nella cittadina belga Ellezelles, in occasione di un funerale.[1] I vari tipi di tossine botuliniche sono stati identificati tra il 1919 e il 1970.[2] Il botulismo infantile invece venne riconosciuto per la prima volta solo nel 1976.[4]
In Italia il botulismo è una malattia a notifica obbligatoria dal 1975.[5] Nel 1990, a seguito della riorganizzazione del sistema informativo delle malattie infettive e diffusive, il botulismo è stato inserito tra le malattie di classe I, per le quali è richiesta la segnalazione da parte del medico all’azienda sanitaria entro 12 ore dalla formulazione della diagnosi, seguendo un flusso informativo che coinvolge la Regione, il Ministero della Salute e l’Istituto Superiore di Sanità.[6]
Dal 1975 al 1991 i casi di botulismo venivano notificati al sistema di sorveglianza nazionale. Tra il 1991 e il 1996 sono state adottate definizioni di caso in accordo con quanto riportato dai Centers for Disease Control and Prevention americani.[5] Nel 1996 il Ministero della Salute ha pubblicato una circolare sulle misure di prevenzione e controllo delle intossicazioni da botulismo[7] adottando specifiche definizioni di caso. Tale circolare è stata aggiornata nel 2012 contemplando le definizioni di caso armonizzate a livello europeo, in ottemperanza alla Decisione della Commissione Europea 2002/253/EC e successive modifiche e integrazioni apportate nel 2003, 2008 e 2009.[7][8]
Le definizioni di caso attualmente in uso a livello nazionale sono conformi alla Decisione di esecuzione (UE) 2018/945.[8][9] Il Ministero della Salute, con la lettera n.702/91.64/2/619 della Direzione Generale Igiene degli Alimenti e Nutrizione del luglio 1988 e successivamente con le Circolari del 1996 e del 2012, ha istituito il Centro Nazionale di Riferimento per il Botulismo (CNRB), presso il Dipartimento di Sicurezza Alimentare, Nutrizione e Sanità Pubblica Veterinaria (DSANV) dell’Istituto Superiore di Sanità. Inoltre il DPCM 03/03/2017 “Identificazione dei sistemi di sorveglianza e dei registri di mortalità, di tumori e di altre patologie”, ha istituito presso l’Istituto Superiore di Sanità il sistema di sorveglianza nazionale del botulismo.[10]
Le modalità di notifica sono state recentemente modificate a seguito della pubblicazione del Decreto del Ministero della Salute 7 marzo 2022 “Revisione del sistema di segnalazione delle malattie infettive (PREMAL)” in ottemperanza al quale, ogni azienda sanitaria può inserire i dati direttamente nella piattaforma PREMAL, aggiornando il sistema in tempo reale.[11]
Nel 2016, al fine di contenere il numero di casi, l'Istituto Superiore della Sanità, attraverso il Centro Nazionale di Riferimento per il Botulismo, ha pubblicato e le "Linee Guida per la corretta preparazione delle conserve alimentari in ambito domestico".[12]
Nel 2015 il CDC diede vita ad una commissione tecnica composto da esperti degli aspetti clinici, epidemiologici e di laboratorio della malattia e dei campi correlati, nonché ad una commissione interna che avevano il compito di redigere le linee guida per il trattamento del botulismo dando priorità alla caratterizzazione dei segni clinici della malattia, alla metodologia per il monitoraggio dei pazienti con sospetta forma d botulismo, ovvero allo stabilire l'efficacia e la sicurezza dell'antitossina. Il lavoro dei due gruppi era incentrato sulle donne in gravidanza e i bambini. Durante tutte le fasi di stesura del documento i due gruppi riportavano ad una commissione composta da rappresentanti delle agenzie federali, inclusi l'Assistant Secretary for Preparedness and Response, la Biomedical Advanced Research and Development Agency il Dipartimento della Sicurezza Nazionale, la Food and Drug Administration (FDA) e i National Institutes of Health.[13]
Il documento finale si basa su sei revisioni sistematiche degli aspetti clinici della malattia, botulismo infantile, botulismo in gravidanza, studi epidemiologici dei focolai di botulismo, l'efficacia dell'antitossina e le reazioni allergiche all'antitossina.[14][15][16] Vennero pubblicate le revisioni e altri nove manoscritti su vari argomenti collegati alla malattia.[13][17][18][19]
In Svizzera vige l’obbligo di dichiarazione entro due ore per i casi di botulismo alimentare. I medici che hanno il sospetto di botulismo alimentare sono tenuti a dichiararlo immediatamente al medico cantonale e all'Ufficio Federale della Sanità Pubblica al fine di identificare rapidamente l’alimento contaminato e a prevenire ulteriori casi d'intossicazione. Per il botulismo da ferita e infantile non vi è invece obbligo di notifica.[20]
Epidemiologia
[modifica | modifica wikitesto]Tra il 1920 e il 2014 sono stati 197 i casi a livello mondiale di botulismo alimentare, con il maggior numero di casi registrati negli Stati Uniti. I dati dimostrano che la tossina di tipo A è responsabile del 34% dei casi, la B per il 16%, l'E per il 17% e la F per l'1%. Una media del 34% dei casi ha avuto necessità della ventilazione meccanica.[3] Gli unici casi di botulismo umano legato alla tossina di tipo C e D sono stati registrati negli anni '50.[21][22]
Secondo dati del ECDC, in Europa i casi di botulismo sono generalmente bassi: 200 casi all'anno (0,03 casi ogni 100.000 persone). I tassi maggiori nel periodo 2007-2017 si sono registrati in Polonia e Lituania. Il maggior numero di casi è legato ad infezioni da ferita in tossicodipendenti. Il botulismo infantile, è raro e affligge bambini al di sotto dei due anni di età, principalmente sotto i 6 mesi.[23]
L'Italia è tra i paesi con il più alto numero di casi di botulismo alimentare: dal 1986 al 30 settembre 2022 sono stati confermati 406 incidenti che hanno coinvolto 599 persone. Il botulismo rimane un problema di salute pubblica, soprattutto nelle regioni meridionali a causa della tradizione consolidata di preparare le conserve alimentari in casa. Gli alimenti maggiormente coinvolti appartengono alla categoria delle conserve di vegetali in olio (47,7%), conserve vegetali in acqua/salamoia (25,5%), conserve di carne (7,8%), conserve di pesce (7,8%), prosciutto (4,6%) salami e salsicce (3,3%), conserve di formaggio (2,0%), alimenti macrobiotici (1,3%). Le preparazioni più frequentemente implicate sono le conserve di funghi in olio di prodizione domestica. Sono altresì molto frequenti le conserve di olive e di cime di rapa.[24]
In Svizzera il botulismo è molto raro: si registrano uno o due casi l’anno.[20]
Negli Stati Uniti:[4]
- i casi di botulismo alimentare sono generalmente 110 l'anno in 46 stati, inclusi Porto Rico e Washington DC. California, Washington, Colorado, Oregon e Alaska sono gli stati in cui sono stati registrati circa il 50% di tutti i casi dal 1950. In Alaska questa forma di botulismo è un problema di salute pubblica tra i nativi.
- i casi di botulismo infantile sono generalmente 110 l'anno con un'età media del paziente di 13 settimane. Maschi e femmine ne sono affetti in egual misura. I bambini affetti generalmente hanno un peso maggiore alla nascita, nascono da genitori di razza caucasica, in età avanzata e di educazione superiore, sono allattati al seno, nati da una normale gravidanza, e senza anomalie congenite. Cluster di casi sono stati identificati in aree suburbane negli stati orientali e in alcune piccole cittadine e aree rurali occidentali.
- i casi di botulismo da ferita sono circa 110 l'anno. I pazienti hanno un'età compresa tra i 23 e i 58 anni con un'età media di circa 41. Ne sono maggiormente affette le donne. Gli stati principalmente afflitti sono quelli occidentali, specialmente la California dove, tra gli anni '80 e '90, il numero di casi è aumentato a causa dell'aumento dell'uso di eroina.
In Taiwan, tra il 2007 e il 2016 sono stati confermati 46 casi totali con un picco di 11 casi l'anno nel 2008 e ne 2011.[25]
Eziologia
[modifica | modifica wikitesto]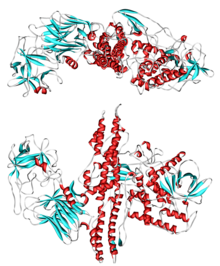
Gli agenti eziologici della malattia sono le tossine botuliniche (BoNT), di cui esistono 9 forme diverse, che in funzione della loro variabilità di sequenza possono essere classificate in oltre 40 sub-tipi,[1] :[26]
- tipo A, B, E, F, G e ibrido F/A -> responsabili delle forme di botulismo nell'uomo
- tipo C e D -> responsabili delle forme di botulismo negli animali (cavalli, mucche, anatre e polli)
- tipo X
Si tratta di proteine globulari che si disattivano al calore, resistenti alla degradazione da parte dell'acidità gastrica e degli enzimi proteolitici, che vengono prodotte naturalmente dai ceppi batterici appartenenti al genere Clostridium e denominati clostridi produttori di BoNT (es. C. baratii e C. butyricum).[2][27][28] Generalmente i ceppi batterici di C. botulinum producono un solo tipo di tossina, ma sono stati identificati ceppi in grado di produrne anche due.[29] Negli ultimi anni, grazie al sequenziamento genetico, sono state identificate due proteine simili alle tossine botuliniche in ceppi di C. botulinum e Enterococcus faecium.[30][31]
La tossina dopo essere penetrata nell'organismo viene trasportata alle terminazioni nervose colinergiche periferiche, incluse le giunzioni neuromuscolari, le terminazioni nervose postgangliniche parasinergiche e i gangli periferici.[32] A livello delle giunzioni neuromuscolari la tossina botulinica attiva una serie di reazioni che includono:[33]
- il legame con catene pesanti a livello del neurone
- trasporto all'interno della cellula mediante endocitosi mediata da recettori
- traslocazione nel citosol
- scissione di specifiche proteine che intervengono nel rilascio dell'acetilcolina
Quali proteine siano interessate dipende da quale tipo di tossina è coinvolta. Le dimensioni della tossina sono probabilmente responsabili della sua incapacità di attraversare la barriera emato-encefalica.[32]
La tossina botulinica di tipo A è responsabile dei casi più gravi della malattia, mentre quella di tipo B ha effetti più leggeri.[14][34][35] Ricerche condotte in laboratorio su tessuti umani dimostrano che la tossina botulinica di tipo C blocca la trasmissione neuromuscolare, ma non viene assorbita a livello gastrointestinale.[36][37] Non sono mai stati riportati casi di botulismo umano legato alla tossina G.[2] La tossina di tipo E è generalmente collegata al consumo di pesce e provoca forme di botulismo di diversa gravità che spesso includono sintomi intestinali.[35][38][39] Casi legati alla tossina di tipo F sono molto rari e comportano una progressione molto rapida dei sintomi, una paralisi estesa ed insufficienza respiratoria con tempi di recupero più rapidi.[40][41]
La DL50 per la tossina botulinica cristallina purificata di tipo A per un uomo di 70 kg è stimata pari a 70 μg per somministrazione orale e 0,80 – 0.90 μg se inalata.[42]
Nonostante i segni clinici e i sintomi siano sempre gli stessi, si distinguono sei diverse forme di botulismo umano in base alla via d'ingresso della tossina nell'organismo:[2][11][27][43]
- botulismo alimentare legato all'ingestione di cibi contaminati
- botulismo da ferita legato alla colonizzazione delle ferite ad opera del C. botulinum e alla successiva produzione di tossine in situ
- botulismo infantile legato alla colonizzazione del lume intestinale e alla conseguente produzione di tossine nei bambini, specialmente dopo l'ingestione di miele
- botulismo da colonizzazione intestinale dell’adulto forma di botulismo molto rara, simile al botulismo infantile, che colpisce invece soggetti adulti
- botulismo iatrogeno conseguente l'uso non corretto delle tossine botuliniche per scopi terapeutici o cosmetici
- botulismo da inalazione di BoNT, accidentalmente o deliberatamente rilasciate, legate all'inalazione della tossina sottoforma di aerosol
La malattia non viene trasmessa da persona a persona.[4]
Botulismo animale
[modifica | modifica wikitesto]Gli animali possono contrarre la malattia ingerendo la tossina o il batterio che la produce. L'infezione viene anche trasmessa dai vermi necrofagi che si cibano delle carcasse di animali infetti accumulando la tossina nel proprio organismo.[44]
Il cavallo risulta essere la specie maggiormente suscettibile alla malattia che si presenta unicamente in tre forme: alimentare (la più diffusa), da ferita e da colonizzazione intestinale. La prognosi è raramente favorevole con la maggior parte degli animali che devono essere abbattuti poche ore dopo la comparsa dei sintomi. La prognosi differenziale nei cavalli deve considerare anche la disfagia e la debolezza neuromuscolare simmetrica.[45]
Ogni anno sono circa 10.000-50.000 i volatili affetti dalla malattia, per la maggior parte si tratta di anatre, benché vi siano anche casi di botulismo in strolaghe, oche e gabbiani. Cani, gatti e maiali sono particolarmente resistenti. I sintomi includono:[44]
- debolezza progressiva
- paralisi flaccida dei muscoli scheletrici
- paralisi respiratoria
- paralisi cardiaca
Il botulismo legato alla tossina di tipo C è comune tra le gli uccelli acquatici nella tarda estate, mentre quella di tipo E colpisce soprattutto le specie dei Grandi Laghi in autunno.[44]
Patogenesi
[modifica | modifica wikitesto]
Uno studio italiano ha dimostrato che esistono alcuni fattori di rischio per la malattia:[11]
- i casi di botulismo tra gli studenti fuori sede riguardano quasi esclusivamente studenti maschi che dalle regioni meridionali si spostano per motivi di studio al nord e portano con sé o si fanno mandare conserve alimentari preparate in casa
- casi di botulismo sono stati registrati fra la popolazione immigrata, soprattutto tra la popolazione maschile nei periodi successivi alle vacanze natalizie e alle ferie estive, a causa di prodotti tipici dei Paesi d'origine che sono relativamente sicuri nei Paesi di produzione, soprattutto se freddi, ma possono diventare pericolosi se conservati a temperature inappropriate per lunghi periodi
- sono stati registrati casi di botulismo correlati al consumo di alimenti multi-ingrediente, fenomeno quasi esclusivamente correlato al consumo di panini farciti in cui sono presenti salse e creme preparate a partire da componenti che presentano caratteristiche chimico-fisiche molto diverse e che possono diventare pericolosi se mescolati in maniera inappropriata
- nell’ampio panorama di prodotti alimentari etnici quelli che destano maggiore preoccupazione sono quelli fermentati, perché spesso conservati a temperatura ambiente per mesi oppure anni. Qualora la fermentazione venga condotta correttamente, soprattutto nelle fasi iniziali, i prodotti che ne derivano sono sicuri, mentre se le ricette tradizionali vengano rivisitate diminuendo ad esempio i quantitativi di sale o di aceto per ottenere prodotti più gradevoli al palato, possono innescarsi processi fermentativi non corretti o addirittura può essere favorito lo sviluppo di microrganismi patogeni
Secondo il CDC altri fattori di rischio sono:[46]
- l'assunzione di droghe
- bere bevande alcoliche fatte in casa
- mangiare cibi contaminati
- sottoporsi a procedure estetiche che comportano l'iniezione della tossina in quantità rilevanti
Clinica
[modifica | modifica wikitesto]La diagnosi è essenzialmente clinica e si basa sull’attenta osservazione dei segni clinici e dei sintomi riferiti dal paziente, nonché della sua storia alimentare.[1]
Segni e sintomi
[modifica | modifica wikitesto]
Segni e sintomi comuni della malattia sono:[47]
- difficoltà di deglutizione
- debolezza muscolare
- midriasi bilaterale
- diplopia
- ptosi
- vista offuscata
- disartria
- difficoltà respiratorie
- difficoltà nel movimento oculare

Segni e sintomi del botulismo alimentare sono:[47]
Sintomi del botulismo infantile sono:[47]
- costipazione
- difficoltà nell'alimentarsi
- palpebre cadenti
- pupille poco reattive
- ridotte espressioni facciali
- pianto debole che suona diverso dal normale
Nel caso del botulismo alimentare i sintomi si presentano generalmente in un arco temporale che va da poche ore (6 ore) a oltre una settimana dopo il consumo dell’alimento contaminato (15 giorni). Tuttavia, nei casi di botulismo alimentare che si verificano in Italia la sintomatologia compare mediamente nell’arco di 24-72 ore. Prima compaiono i sintomi più severa sarà la malattia.
Nelle forme più gravi si assiste all’insufficienza respiratoria che può avere esito fatale per blocco della conduzione nervosa ai muscoli responsabili della respirazione. La sintomatologia ha una progressione simmetrica, ovvero interessa sia l’emisfero destro che quello sinistro del corpo, discendente, parte dalla testa, al collo, al torace, fino alla paralisi degli arti, e si manifesta con una paralisi flaccida.[1]

Esami di laboratorio e strumentali
[modifica | modifica wikitesto]La diagnosi di laboratorio consiste nella ricerca delle tossine botuliniche nel sangue, nelle feci e nei residui alimentari consumati dal paziente, nonché nella determinazione dei clostridi produttori di tossine botuliniche nelle feci e nei residui alimentari. Possono essere di supporto alla diagnosi alcuni test strumentali come l’elettromiografia. Le analisi biochimiche e cliniche generalmente non danno risposte suggestive.[1]
Diagnosi differenziale
[modifica | modifica wikitesto]Soprattutto all’esordio, può essere confusa con altre patologie a carico del sistema nervoso come la sindrome di Guillain-Barrè, miastenia gravis, sindrome di Eaton Lambert, paralisi provocata da zecche, avvelenamento da biotossine presenti nei mitili, poliomielite e ictus. Il sospetto diagnostico formulato dal medico, per poter diventare diagnosi definitiva deve essere confermato in laboratorio.[1]
Trattamento
[modifica | modifica wikitesto]Trattamento farmacologico
[modifica | modifica wikitesto]La terapia specifica consiste nella somministrazione di un siero iperimmune (antitossina eptavalente equina da A a G) che deve essere somministrato il prima possibile, senza attendere gli esiti della diagnosi di laboratorio e in ambiente controllato. Pertanto il paziente necessita del ricovero ospedaliero, possibilmente in terapia intensiva.[1]

In Italia, l’antidoto è stato incluso nella scorta nazionale antidoti e può essere distribuito in tutto il territorio nazionale nell’arco di poche ore, previa richiesta motivata al Ministero della Salute.[27]
Negli Stati Uniti l'antitossina botulinica è disponibile gratuitamente a seguito di segnalazione medica al governo federale. I vari dipartimenti della salute e il CDC forniscono consulenza medica d'emergenza 24 ore su 24 e facilitano la distribuzione dell'antitossina per il trattamento delle forme di botulismo non infantili per cui interviene invece il California Department of Public Health Infant Botulism Treatment and Prevention Program.[28]
Prognosi
[modifica | modifica wikitesto]La maggior parte dei pazienti va incontro a guarigione dopo settimane o mesi di terapia di supporto.[11] I pazienti in cui si presentano sintomi respiratori gravi possono anche andare in contro alla morte.[47]
Prevenzione
[modifica | modifica wikitesto]Dal momento che le spore dei clostridi produttori di tossine botuliniche sono ubiquitarie, possono contaminare anche gli alimenti e le materie prime di partenza.[1] Dal momento che una delle condizioni imprescindibili affinché le spore siano in grado di svilupparsi è l’assenza di ossigeno, gli alimenti freschi (insalata, pane, pasta, ecc.) non sono a rischio. Sono a rischio, invece, le conserve e le semi-conserve non acide (pH > 4,5) o che non hanno subito trattamenti di acidificazione/fermentazione. Le conserve di produzione industriale generalmente non sono pericolose perché le tecnologie di produzione sono ben standardizzate e consentono il controllo dello sviluppo e della tossinogenesi dei clostridi produttori di tossine botuliniche.[1]
Il botulismo alimentare è prevenibile prendendo le accurate cautele nel preparare il cibo, specialmente le conserve e i cibi in scatola. Particolare attenzione deve essere posta alla preparazione di cibi con poca acidità (vegetali, fichi, carni, pollame, pesci, frutti di mare e alcune varietà di pomodori).[48]
Legislazione
[modifica | modifica wikitesto]Il C. botulinum è inserito nell’ elenco delle zoonosi e degli agenti zoonotici da sottoporre a sorveglianza in funzione della situazione epidemiologica del Decreto Legislativo 191 del 4 aprile 2006 “Attuazione della direttiva 2003/99/CE sulle misure di sorveglianza delle zoonosi e degli agenti zoonotici”.[49]
Note
[modifica | modifica wikitesto]- ^ a b c d e f g h i j k EpiCentro, Botulismo alimentare - EpiCentro - Istituto Superiore di Sanità, su www.epicentro.iss.it. URL consultato il 3 giugno 2024.
- ^ a b c d e (EN) J. Sobel, Botulism, in Clinical Infectious Diseases, vol. 41, n. 8, 15 ottobre 2005, pp. 1167–1173, DOI:10.1086/444507. URL consultato il 4 giugno 2024.
- ^ a b (EN) Shannon Fleck-Derderian, Manjunath Shankar e Agam K Rao, The Epidemiology of Foodborne Botulism Outbreaks: A Systematic Review, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S73–S81, DOI:10.1093/cid/cix846. URL consultato il 3 giugno 2024.
- ^ a b c (EN) CDC Botulism | Epidemiological Overview for Clinicians, su emergency.cdc.gov, 21 febbraio 2019. URL consultato il 3 giugno 2024.
- ^ a b Anniballi F, Auricchio B, Fiore A, Lonati D, Locatelli CA, Lista F, Fillo S, Mandarino G, De Medici D., Botulism in Italy, 1986 to 2015, in Euro Surveill, vol. 22, n. 4, 2017, p. 30550, DOI:10.2807/1560-7917..
- ^ Maria Pia Fantini, Laura Dallolio e Giuliana Fabbri, Igiene e sanità pubblica. Appunti sui temi dell'epidemiologia, delle malattie infettive, delle vaccinazioni e della prevenzione, 1º marzo 2012, DOI:10.15651/978-88-748-8496-4. URL consultato il 4 giugno 2024.
- ^ a b La riforma delle misure di prevenzione patrimoniali ad opera della l. 161/2017 tra istanze efficientiste e tentativi incompiuti di giurisdizionalizzazione del procedimento di prevenzione, in Archivio penale, 2018, DOI:10.12871/978883318026719. URL consultato il 4 giugno 2024.
- ^ a b Commissione Europea, Decisione 2002/253/EC della Commissione del 19 marzo 2002, che stabilisce la definizione dei casi ai fin della dichiarazione delle malattie trasmissibili alla rete di sorveglianza comunitaria istituita ai sensi della decisione n. 2119/98/CE del Parlamento europeo e del Consiglio., in Gazzetta Ufficiale, L 086, 3 aprile 2002.. URL consultato il 4 giugno 2024.
- ^ Commissione Europea, Decisione di esecuzione (UE) 2018/945 della Commissione del 22 giugno 2018 relativa alle malattie trasmissibili e ai problemi sanitari speciali connessi da incorporare nella sorveglianza epidemiologica, nonché alle pertinenti definizioni di caso., in Gazzetta ufficiale dell'Unione europea, L 170/1, 6 luglio 2018. URL consultato il 4 giugno 2024.
- ^ Centro nazionale di riferimento, su ISS. URL consultato il 4 giugno 2024.
- ^ a b c d Botulismo umano, su ISS. URL consultato il 4 giugno 2024.
- ^ Istituto Superiore di Sanità, Centro Nazionale di Riferimento per il Botulismo e Centro Antiveleni e Centro Nazionale di Informazione Tossicologica di Pavia, LINEE GUIDA PER LA CORRETTA PREPARAZIONE DELLE CONSERVE ALIMENTARI IN AMBITO DOMESTICO, 2016. URL consultato il 4 giugno 2024.
- ^ a b (EN) Jeremy Sobel e Agam K Rao, Making the Best of the Evidence: Toward National Clinical Guidelines for Botulism, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S1–S3, DOI:10.1093/cid/cix829. URL consultato il 4 giugno 2024.
- ^ a b (EN) Kevin Chatham-Stephens, Shannon Fleck-Derderian e Shacara D Johnson, Clinical Features of Foodborne and Wound Botulism: A Systematic Review of the Literature, 1932–2015, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S11–S16, DOI:10.1093/cid/cix811. URL consultato il 4 giugno 2024.
- ^ (EN) Shannon Fleck-Derderian, Manjunath Shankar e Agam K Rao, The Epidemiology of Foodborne Botulism Outbreaks: A Systematic Review, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S73–S81, DOI:10.1093/cid/cix846. URL consultato il 4 giugno 2024.
- ^ (EN) Stephanie E Griese, Hannah M Kisselburgh e Michael T Bartenfeld, Pediatric Botulism and Use of Equine Botulinum Antitoxin in Children: A Systematic Review, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S17–S29, DOI:10.1093/cid/cix812. URL consultato il 4 giugno 2024.
- ^ (EN) Agam K Rao, Neal H Lin e Kelly A Jackson, Clinical Characteristics and Ancillary Test Results Among Patients With Botulism—United States, 2002–2015, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S4–S10, DOI:10.1093/cid/cix935. URL consultato il 4 giugno 2024.
- ^ (EN) Alison Laufer Halpin, Jessica M Khouri e Jessica R Payne, Type F Infant Botulism: Investigation of Recent Clusters and Overview of This Exceedingly Rare Disease, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S92–S94, DOI:10.1093/cid/cix818. URL consultato il 4 giugno 2024.
- ^ (EN) Agam K Rao, Maroya Walters e Julia Hall, Outbreak of Botulism Due to Illicit Prison-Brewed Alcohol: Public Health Response to a Serious and Recurrent Problem, in Clinical Infectious Diseases, vol. 66, suppl_1, 1º gennaio 2018, pp. S85–S91, DOI:10.1093/cid/cix936. URL consultato il 4 giugno 2024.
- ^ a b Ufficio federale della sanità pubblica UFSP, Botulismo, su www.bag.admin.ch. URL consultato il 3 giugno 2024.
- ^ John E. Atwell, Existence precedes essence, in Man and World, vol. 2, n. 4, 1969-11, pp. 580–591, DOI:10.1007/bf01249074. URL consultato il 4 giugno 2024.
- ^ Jean-Charles Duclos-Vallée, Une succession de maladies autoimmunes, in Gastroentérologie Clinique et Biologique, vol. 31, n. 3, 2007-03, pp. 354–356, DOI:10.1016/s0399-8320(07)89389-4. URL consultato il 4 giugno 2024.
- ^ (EN) Facts about botulism, su www.ecdc.europa.eu, 31 maggio 2012. URL consultato il 3 giugno 2024.
- ^ EpiCentro, Botulismo alimentare aspetti epidemiologici, su www.epicentro.iss.it. URL consultato il 3 giugno 2024.
- ^ (EN) Botulism, su www.cdc.gov.tw. URL consultato il 3 giugno 2024.
- ^ (EN) Bao-Chung Chen, Yao-Ching Huang e Shi-Hao Huang, Epidemiology and risk factors for notifiable Clostridium botulinum infections in Taiwan from 2003 to 2020, in Medicine, vol. 101, n. 42, 21 ottobre 2022, pp. e31198, DOI:10.1097/MD.0000000000031198. URL consultato il 3 giugno 2024.
- ^ a b c Fabrizio Anniballi, Antonino Bella e Concetta Scalfaro, Il sistema di sorveglianza nazionale del botulismo: i dati in Italia dal 2001 al 2020, in Bollettino epidemiologico nazionale, 2022. URL consultato il 4 giugno 2024.
- ^ a b Agam K. Rao, Jeremy Sobel e Kevin Chatham-Stephens, Clinical Guidelines for Diagnosis and Treatment of Botulism, 2021, in MMWR. Recommendations and Reports, vol. 70, n. 2, 7 maggio 2021, pp. 1–30, DOI:10.15585/mmwr.rr7002a1. URL consultato il 4 giugno 2024.
- ^ (EN) Susan E. Maslanka, Carolina Lúquez e Janet K. Dykes, A Novel Botulinum Neurotoxin, Previously Reported as Serotype H, Has a Hybrid-Like Structure With Regions of Similarity to the Structures of Serotypes A and F and Is Neutralized With Serotype A Antitoxin, in Journal of Infectious Diseases, vol. 213, n. 3, 1º febbraio 2016, pp. 379–385, DOI:10.1093/infdis/jiv327. URL consultato il 4 giugno 2024.
- ^ (EN) Sicai Zhang, Geoffrey Masuyer e Jie Zhang, Identification and characterization of a novel botulinum neurotoxin, in Nature Communications, vol. 8, n. 1, 3 agosto 2017, DOI:10.1038/ncomms14130. URL consultato il 4 giugno 2024.
- ^ (EN) Jason Brunt, Andrew T. Carter e Sandra C. Stringer, Identification of a novel botulinum neurotoxin gene cluster in Enterococcus, in FEBS Letters, vol. 592, n. 3, 2018-02, pp. 310–317, DOI:10.1002/1873-3468.12969. URL consultato il 4 giugno 2024.
- ^ a b (EN) Yann Humeau, Frédéric Doussau e Nancy J Grant, How botulinum and tetanus neurotoxins block neurotransmitter release**This paper is dedicated to the memory of Heiner Niemann., in Biochimie, vol. 82, n. 5, 2000-05, pp. 427–446, DOI:10.1016/S0300-9084(00)00216-9. URL consultato il 4 giugno 2024.
- ^ J. G. COLLEE, Botulism. The organism, its toxins, the disease: By LOUIS DS. SMITH. 1977. Springfield, Illinois: Charles C. Thomas. Pp. vii and 236. US$l8.75., in Journal of Medical Microbiology, vol. 11, n. 2, 1º maggio 1978, pp. 220–220, DOI:10.1099/00222615-11-2-220. URL consultato il 4 giugno 2024.
- ^ (EN) James M. Hughes, Clinical Features of Types A and B Food-borne Botulism, in Annals of Internal Medicine, vol. 95, n. 4, 1º ottobre 1981, pp. 442, DOI:10.7326/0003-4819-95-4-442. URL consultato il 4 giugno 2024.
- ^ a b (EN) B. A. Woodruff, P. M. Griffin e L. M. McCroskey, Clinical and Laboratory Comparison of Botulism from Toxin Types A, B, and E in the United States, 1975-1988, in Journal of Infectious Diseases, vol. 166, n. 6, 1º dicembre 1992, pp. 1281–1286, DOI:10.1093/infdis/166.6.1281. URL consultato il 4 giugno 2024.
- ^ N. Bakry, J. Coffield e A.B. Maksymowych, The structure and mechanism of action of botulinum toxin, in Toxicon, vol. 34, n. 3, 1996-03, pp. 294, DOI:10.1016/0041-0101(96)80883-x. URL consultato il 4 giugno 2024.
- ^ (EN) Roberto Eleopra, Valeria Tugnoli e Rocco Quatrale, Botulinum neurotoxin serotypes A and C do not affect motor units survival in humans: an electrophysiological study by motor units counting, in Clinical Neurophysiology, vol. 113, n. 8, 2002-08, pp. 1258–1264, DOI:10.1016/S1388-2457(02)00103-7. URL consultato il 4 giugno 2024.
- ^ M. GLENN KOENIG, ANDERSON SPICKARD e MATTEO A. CARDELLA, CLINICAL AND LABORATORY OBSERVATIONS ON TYPE E BOTULISM IN MAN, in Medicine, vol. 43, n. 5, 1964-09, pp. 517–546, DOI:10.1097/00005792-196409000-00001. URL consultato il 4 giugno 2024.
- ^ IVAN C. HALL, FURTHER OUTBREAKS OF BOTULISM IN THE ROCKY MOUNTAIN REGION*, in American Journal of Epidemiology, vol. 17, n. 1, 1933-01, pp. 235–251, DOI:10.1093/oxfordjournals.aje.a117904. URL consultato il 4 giugno 2024.
- ^ (EN) A. Gupta, C. J. Sumner e M. Castor, Adult botulism type F in the United States, 1981–2002, in Neurology, vol. 65, n. 11, 13 dicembre 2005, pp. 1694–1700, DOI:10.1212/01.wnl.0000187127.92446.4c. URL consultato il 4 giugno 2024.
- ^ Jeremy Sobel, Tracy Dill e Christina L. Kirkpatrick, Clinical Recovery and Circulating Botulinum Toxin Type F in Adult Patient, in Emerging Infectious Diseases, vol. 15, n. 6, 2009-06, pp. 969–971, DOI:10.3201/eid1506.070571. URL consultato il 4 giugno 2024.
- ^ (EN) Stephen S. Arnon, Robert Schechter e Thomas V. Inglesby, Botulinum Toxin as a Biological Weapon: Medical and Public Health Management, in JAMA, vol. 285, n. 8, 28 febbraio 2001, pp. 1059, DOI:10.1001/jama.285.8.1059. URL consultato il 4 giugno 2024.
- ^ Botulismo - Malattie infettive, su Manuali MSD Edizione Professionisti. URL consultato il 4 giugno 2024.
- ^ a b c (EN) admin, Botulism, su cwhl.vet.cornell.edu, 22 dicembre 2016. URL consultato il 4 giugno 2024.
- ^ (EN) C. H. Stratford, I. G. Mayhew e N. P. H. Hudson, Equine botulism: A clinical approach to diagnosis and management, in Equine Veterinary Education, vol. 26, n. 8, 2014-08, pp. 441–448, DOI:10.1111/eve.12198. URL consultato il 4 giugno 2024.
- ^ (EN) CDC, People at Increased Risk for Botulism, su Botulism, 9 maggio 2024. URL consultato il 4 giugno 2024.
- ^ a b c d (EN) CDC, Symptoms of Botulism, su Botulism, 19 aprile 2024. URL consultato il 4 giugno 2024.
- ^ (EN) CDC, Botulism Prevention, su Botulism, 16 maggio 2024. URL consultato il 4 giugno 2024.
- ^ Dlgs 191/06, su www.parlamento.it. URL consultato il 4 giugno 2024.
Bibliografia
[modifica | modifica wikitesto]- Epidemiologic Notes and Reports Fish Botulism --- Hawaii, 1990
- Wound Botulism -- California, 1995
- Foodborne Botulism -- Oklahoma, 1994
- Fillo S, Giordani F, Tonon E, Drigo I, Anselmo A, Fortunato A, Lista F, Bano L. Extensive Genome Exploration of Clostridium botulinum Group III Field Strains. 2021 13;9(11):2347.
- Woudstra C, Mäklin T, Derman Y, Bano L, Skarin H, Mazuet C, Honkela A, Lindström M. Closing Clostridium botulinum Group III Genomes Using Long-Read Sequencing. Microbiol Resour Announc. 2021; 10(22):e0136420.
- Drigo I, Tonon E, Pascoletti S, Anniballi F, Kalb SR, Bano L. Detection of Active BoNT/C and D by EndoPep-MS Using MALDI Biotyper Instrument and Comparison with the Mouse Test Bioassay. Toxins (Basel). 2020; 13(1):10.
- Auricchio,B.; Scalfaro,C.; Bano,L.; Bilei,S.; De Santis,P.; Dorner,B.; Dorner,M.; Drigo,I.; Engelsma,M.; Fach,P.; Hedeland,M.; Koene, M.; Korkeala,H.; Lindström,M.; Seyboldt,C.; Skarin,H.; Tevell Åberg,A.; Woudstra,C.; Yagmur,D.; Anniballi,F. (2019). International Proficiency Test of the AniBotNet Project on the Detection of Botulinum Neurotoxins type C, D, C/D, D/C. 2019, Botulism Workshop, Abstract book, 36, Maisons-Alfort, France
- Auricchio,B.; Scalfaro,C.; Vicenza,T.; Bano,L.; Bilei,S.; Chemaly,M.; De Santis,P.; Dorner,B.; Dorner,M.; Drigo,I.; Engelsma,M.; Fach,P.; Hedeland,M.; Koene,M.; Korkeala,A.; Le Maréchal,C.; Lindström,M.; Seyboldt,C.; Skarin,H.; Souillard,R.; Tevell Åberg,A.; Woudstra,C.; Yagmur,D.; Anniballi,F. (2019). Multilocus Variable-Number of Tandem-Repeat Analysis as a tool for Clostridium botulinum group III subtyping. 2019, Botulism Workshop, Abstract book, 35, Maisons-Alfort, France
- Bano,L.; Ferro,T.; Guolo,A.; Bacchin,C.; Brunetta,R.; Anniballi,F.; Bilei,S.; Koene,M.; Le Maréchal,C.; Skarin,H.; Seyboldt,C.; Agnoletti,F. (2019). Antimicrobial susceptibility of Clostridium botulinum group III. 2019, 11th International Conferences on the Molecular Biology and Pathogenesis of the Clostridia, Clostpath 11, 244-245, Leiden, The Netherlands
- Bano,L.; Tonon,E.; Drigo,I.; Pirazzini,M.; Guolo,A.; Farina,G.; Agnoletti,F.; Montecucco,C. (2018). Detection of Clostridium tetani Neurotoxins Inhibited In Vivo by Botulinum Antitoxin B: Potential for Misleading Mouse Test Results in Food Controls. Toxins, 2018, 10, 6
- Drigo,I.; Zandonà,L.; Tonon,E.; Pascoletti,S.; Agnoletti,F.; Bano,L. (2018). Comparazione tra mouse test e Endopep-MS nella ricerca di tossina botulinica. 2018, XVIII Congresso Nazionale S.I.Di.L.V. – Volume degli Atti, 214-216, Perugia, Italy
- Viel,L.; Drigo,I.; Tonon,E.; Genovese,S.; Zandonà,L.; Brunetta,R.; Agnoletti,F.; Farina,G.; Bano,L. (2018). Falsa positività per Clostridium botulinum in alimenti: la neurotossina che non ti aspetti. 2018, XVIII Congresso Nazionale S.I.Di.L.V. – Volume degli Atti, 81-82, Perugia, Italy
- Bano,L.; Drigo,I.; Tonon,E.; Pascoletti,S.; Puiatti,C.; Anniballi,F.; Auricchio,B.; Lista,F.; Montecucco,C.; Agnoletti,F. (2017). Identification and characterization of Clostridium botulinum group III field strains by matrix-assisted laser desorption-ionization time-of-flight mass spectrometry (MALDI-TOF MS). Anaerobe, 2017, 48, 126-134, Elsevier Ltd, England
- Lista,F.; Fillo,S.; Giordani,F.; Petralito,G.; Cerreto,G.; Bano,L. (2017). Extensive genome exploration of Clostridium botulinum group III field strains. 2017, 115, Burlingame, CA, USA
- Peck,M.W.; Smith,T.J.; Anniballi,F.; Austin,J.W.; Bano,L.; Bradshaw,M.; Cuervo,P.; Cheng,L.W.; Derman,Y.; Dorner,B.G.; Fisher,A.; Hill,K.K.; Kalb,S.R.; Korkeala,H.; Lindstrom,M.; Lista,F.; Luquez,C.; Mazuet,C.; Pirazzini,M.; Popoff,M.R.; Rossetto,O.; Rummel,A.; Sesardic,D.; Singh,B.R.; Stringer,S.C. (2017). Historical Perspectives and Guidelines for Botulinum Neurotoxin Subtype Nomenclature. Toxins, 2017, 9, 1, 10.3390/toxins9010038, Switzerland
- Drigo,I.; Tonon,E.; Pascoletti,S.,Puiatti,C.; Agnoletti,F.; Bano,L. (2015). Characterization of Clostrisium botulinum field strains of animal origin by MALDI TOF-MS. 2015, CLOSTPATH 2015 9th International Conference on the molecular biology and pathogenesis of the clostridia – Program & Abstracts, 94, Freiburg, Germany
- Aleman, M., Williams, D.C., Jorge, N.E., Magdesian, K.G., Brosnan, R.J., Feary, D.J., Hilton, H.G., Kozikowski, T.A., Higgins, J.K., Madigan, J.E. and LeCouteur, R.A. (2011) Repetitive stimulation of the common peroneal nerve as a diagnostic aid for botulism in foals. J. Vet. Intern. Med. 25, 365-372.
- Rachel Gough, Kate McGovern, Neurological disease in neonatal foals: beyond dummy foal syndrome, UK-Vet Equine, 10.12968/ukve.2022.6.1.12, 6, 1, (12-19), (2022).Carla J. Olave, Kathleen M. Ivester, Laurent L. Couetil, John Burgess, Jae Hong Park, Abhijit Mukhopadhyay, Effects of low‐dust forages on dust exposure, airway cytology, and plasma omega‐3 concentrations in Thoroughbred racehorses: A randomized clinical trial, Journal of Veterinary Internal Medicine, 10.1111/jvim.16598, 37, 1, (338-348), (2022).
- Amy Stieler Stewart, Kathryn L. Wotman, Brittany B. Martabano, Jennifer L. Davis, Ocular Manifestations of Systemic Disease, Equine Ophthalmology, 10.1002/9781119782285.ch13, (721-791), (2022).
- Robert J. Mackay, John R. Middleton, Monica Aleman, Diseases of the Nervous System, Large Animal Internal Medicine, 10.1016/B978-0-323-55445-9.00035-5, (1006-1117.e31), (2020).
- Cecilia Elisabeth Müller, Silage and haylage for horses, Grass and Forage Science, 10.1111/gfs.12387, 73, 4, (815-827), (2018).
- Harold C. McKenzie, Disorders of Foals, Equine Internal Medicine, 10.1016/B978-0-323-44329-6.00020-6, (1365-1459), (2018).
- A. Shnaiderman‐Torban, D. Elad, G. Kelmer, G. Avni, U. Shalit, A. Steinman, An outbreak of equine botulism type D in Israel, Equine Veterinary Education, 10.1111/eve.12725, 30, 11, (594-597), (2017).
- Sevim Kasap, Hasan Batmaz, Meriç Kocatürk, Frank Gessler, Serkan Catık, Onur Topal, Botulism (type A) in a horse - case report, Acta Veterinaria Brno, 10.2754/avb201685010071, 85, 1, (71-76), (2016).
- Shnaiderman‐Torban, A., et al An outbreak of equine botulism type D in Israel. Equine Veterinary Education. 2017
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «botulismo»
Wikizionario contiene il lemma di dizionario «botulismo» Wikimedia Commons contiene immagini o altri file sul botulismo
Wikimedia Commons contiene immagini o altri file sul botulismo
Collegamenti esterni
[modifica | modifica wikitesto]| Controllo di autorità | Thesaurus BNCF 40380 · LCCN (EN) sh85016076 · GND (DE) 4146411-4 · BNF (FR) cb119827885 (data) · J9U (EN, HE) 987007283984805171 |
|---|